感染性心内膜炎 JCS 2026ガイドライン・9年ぶり改訂で現場は何が変わるか

血液培養3セットから Staphylococcus aureus が検出され、経胸壁心エコーで僧帽弁に疣腫。循環器内科からコンサルトが入ります。抗菌薬はセファゾリンでよいか、アミノグリコシドは足すのか、外科紹介はいつか、脳梗塞合併例で手術は遅らせるべきか。これらの判断が一度に問われます。
感染性心内膜炎(IE)は感染症診療のなかでも、抗菌薬の選択・外科紹介のタイミング・画像診断の解釈・予防の適応という複数の軸が同時に問われる疾患です。その国内標準であるJCS「感染性心内膜炎の予防と治療に関するガイドライン」が、2026年3月20日に9年ぶりに全面改訂されました。
9年の間に何が起きたかを振り返ると、国際的には大きな動きが相次いでいました。2023 Duke-ISCVID基準による診断の現代化、ESC 2023による外科適応とタイミングの整理、POET試験による「全員6週間点滴」という前提の見直し、EASE試験と観察研究の蓄積による早期手術の地位確立。JCS 2026はこれらを一気に反映した版になりました。
本記事では改訂内容を「診断」「治療」「外科」「予防」の4軸で整理します。TAVI関連IE(TAVI-PVE)、CIED関連IE(CDRIE)、右心系IE、真菌性IE、感染性脳動脈瘤といった特殊病態はJCS 2026で独立章として扱われており、専門的対応については原文を参照してください。
この記事のポイント
本記事で使用する略語とクラス分類
なぜ今改訂だったのか:9年間に起きたこと
旧版(JCS 2017)から9年の間に、IE診療の前提は大きく書き換えられました。変化を4つに分けて整理しておくと、以降の章の位置づけが理解しやすくなります。
- 画像診断の進化:FDG-PET/CTと心臓CTが人工弁IEの診断精度を大きく引き上げ、Duke基準への組み込みが進んだ
- TAVI・CIEDの普及:経カテーテル弁植込みや心臓デバイスが増え、エコーだけでは捕まえられないIEが一定数存在するようになった
- 治療の多様化:POET試験で「選別された症例では経口スイッチが可能」、EASE試験で「大きな疣腫では早期手術が有利」という2つの大きなエビデンスが出た
- 予防のエビデンス更新:歯科処置前予防の対象と範囲が観察研究の蓄積で再検討された
現代のIEは、エコー所見と血液培養の組み合わせだけでは捌けなくなっています。JCS 2026を読むときに意識すべきは、抗菌薬各論の更新を追うこと以上に、診断の再定義、抗菌薬レジメンの骨格再整理、外科紹介の前倒し化という3つの柱を掴むことです。
診断が変わった:Duke-ISCVID 2023への完全移行
JCS 2026の診断章は、修正Duke基準(2000年版)から2023 Duke-ISCVID基準(Fowlerら、Clin Infect Dis)への完全移行を打ち出しました。2023 Duke-ISCVID本体は新基準の提案文書で、外部妥当性の検証は後続研究に委ねられており、複数の多施設外部検証コホート(Clin Infect Dis 2024など)で感度84.2%(修正Duke 74.9%、ESC 2015 80%に対する相対的改善)・特異度の有意な低下なし、という結果が報告されています。
主な変更点は4つあります。
典型菌リストの拡大
従来の典型菌に加え、新たな病原体群が「典型菌」または「心内人工物がある場合のみ典型」というカテゴリとして整理されました。
| カテゴリ | 菌種 |
|---|---|
| 従来の典型菌(継続) | viridans streptococci, S. gallolyticus, HACEK群, S. aureus, 市中発症の enterococci |
| 新たに追加された典型菌 | S. lugdunensis, enterococci(E. faecalis を含む), S. pneumoniae と S. pyogenes を除く streptococci, Granulicatella と Abiotrophia spp., Gemella spp. |
| 心内人工物がある場合のみ典型 | coagulase-negative staphylococci, Corynebacterium striatum, C. jeikeium, Serratia marcescens, Pseudomonas aeruginosa, Cutibacterium acnes, 非結核性抗酸菌, Candida spp. |
人工弁・人工血管・CIEDを持つ患者で「心内人工物がある場合のみ典型」に該当する菌が検出された場合、旧基準よりも診断的意義が高く評価されるようになりました。
Major / Minor criterionの拡張
Major criterionへの追加としては、まず心臓手術中の肉眼的証拠(vegetation、abscess、pseudoaneurysmの直視)が新たに加わりました。さらに画像診断のMajor criterionに、心臓CTで確認された vegetation・膿瘍・穿孔と、FDG-PET/CTでの人工弁周囲の異常集積(プロステーシス植込みから3か月以降)が正式に組み込まれました。PET/CTは人工弁IE・CIED感染で修正Duke基準の「possible」症例を再分類する最も強力な手段であり、後続の個別患者データメタ解析でも同様の支持が重ねられています。
Minor criterionについても拡張があり、従来の素因項目にCIEDと既往IEが加わり、vascular phenomenaには脳膿瘍と脾膿瘍が追加されました。
血液培養採取要件の緩和
加えて、血液培養の採取要件が緩和されました。旧基準では「12時間以上空けた2セット」「異なる静脈穿刺部位から3セット」といった厳格な時間・穿刺要件がMajor criterion(血液培養陽性)に組み込まれていましたが、2023 Duke-ISCVIDでこの要件は撤廃され、実臨床の迅速化に沿う形になりました。
日本実装の課題:FDG-PET/CT
日本で実装する際の最大の課題は、FDG-PET/CTの保険適用です。人工弁IE疑いでの診療報酬上の扱いは限定的で、「臨床的IE」として抗菌薬治療を継続せざるを得ない症例が現場で残ります。
撮影時には核医学科・放射線科との事前協議が必須です。心筋は生理的にグルコースを取り込むため、そのまま撮像すると弁周囲の異常集積が心筋の生理的集積に紛れてしまい、IEの病変が見えなくなります。これを抑制するために、撮影前の脂肪食(ケト食)負荷や未分画ヘパリン前投与で心筋の生理的なFDG集積を抑える操作が必要で、この前処置プロトコルが診断精度を大きく左右します。造影CTとの組み合わせタイミングも施設ごとに詰めておくと、人工弁周囲の膿瘍や仮性瘤の評価精度が安定します。
抗菌薬治療が変わった:レジメン大幅刷新
JCS 2026の治療章は、9年間の臨床試験・観察研究の蓄積を受けて、複数のレジメンの推奨ランクを動かしました。特に注目すべきは、推奨表で「推奨しない」側に整理された3つです。
感染症コンサルトの現場でも、この領域は議論が残る論点が多く、繰り返し問われるのは「MSSA-IEで内服薬への変更は可能か」「腸球菌IEでAMG併用を回避できるか」の2つです。前者はOPATや退院後フォローの設計上の需要、後者は高齢者・腎機能低下例でのAMG回避需要が背景にあり、JCS 2026の推奨表の方向性はこの2問に対する明確な羅針盤になります。
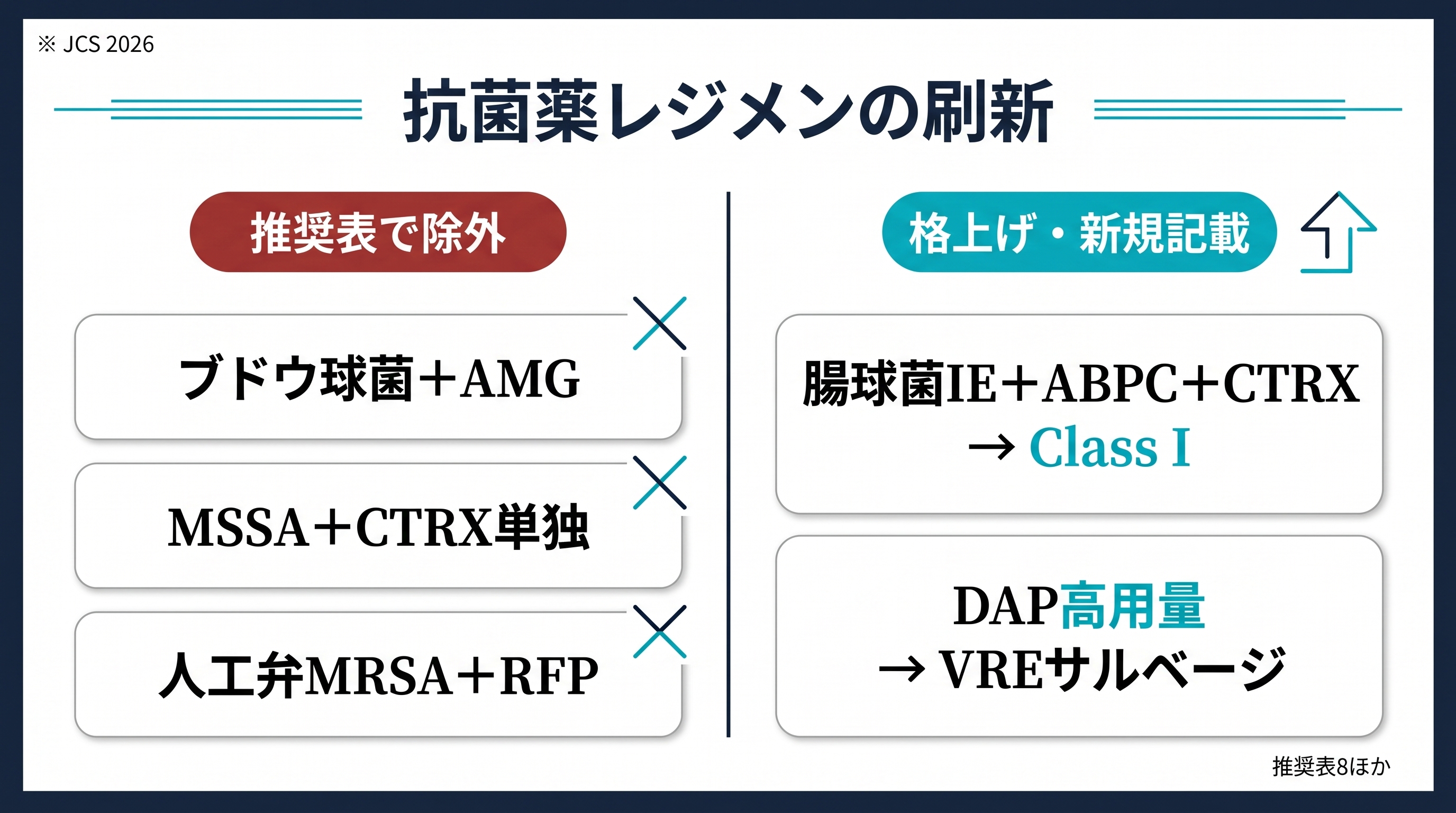
推奨表で「推奨しない」側に整理された3レジメン
ブドウ球菌自己弁IEへのアミノグリコシド(AMG)併用について、JCS 2026の推奨表8(ブドウ球菌による自己弁IEの標的治療)は、セファゾリン単独(クラスI、エビデンスレベルB)を第一選択としたうえで「アミノグリコシド系薬の併用は推奨しない(推奨クラスIII harm、エビデンスレベルC)」と併記しています。短期併用で菌体クリアランスを早める古典的期待に対して、腎障害が有意に増えること、かつ臨床アウトカムの改善を支持する試験が得られていないこと、が背景です。国際的にも慎重論が強まっており、旧版で「初期5日間ゲンタマイシン併用を考慮」とされていた運用はJCS 2026の推奨表上では後退した扱いになります。
同じ推奨表8では、MRSA自己弁IEに対するバンコマイシンとβ-ラクタム系薬の併用も「Class III No benefit(エビデンスレベルC)」と整理されました。CAMERA-2試験(Tong 2020 JAMA)で示された腎障害増加と便益欠如の結果と整合する位置づけです。
MSSA自己弁IEへのセフトリアキソン(CTRX)単独について、JCS 2026推奨表8は「投与は推奨されない(クラスIII No benefit、エビデンスレベルC)」と記載しています。MSSAに対するCTRXの妥当性は以前から議論があり、OPAT運用上の選択肢として使われてきましたが、バイオフィルム下・高菌量環境での有効性に懸念が残ることが背景です。自己弁MSSA-IEの第一選択はセファゾリン(CEZ)で、中枢神経合併症例では髄液移行を重視した併用が必要になります(日本では抗黄色ブドウ球菌ペニシリンであるnafcillin/oxacillinが保険承認されておらず、CEZ高用量にバンコマイシンやメロペネム、セフェピム等を状況に応じて併用する運用が現実的)。この領域はJCS 2026も「エビデンス蓄積が必要」と明記しており、個々の症例で感染症科と循環器科が判断を摺り合わせる運用になります。
人工弁MRSAへのリファンピシン(RFP)併用について、JCS 2026本文は「MRSAによるPVEに対するリファンピシン併用の有効性は、十分なエビデンスがないため本ガイドラインでは推奨していない」と明記しています。バンコマイシン+RFP+GMの3剤併用は人工弁S. aureus IEの古典レジメンでしたが、臨床試験での便益が再現されず、RFP関連の薬物相互作用と肝障害リスクが目立つ結果になっています。バンコマイシン(または DAP)+GM短期併用の判断は個別化されます。
「格上げ」と「新規記載」
腸球菌IE への ABPC+CTRX併用は、Class IIaからClass Iへ格上げされました。高齢者・腎機能低下例でAMG併用が使いにくい背景のもと、ABPC+CTRXの併用療法は治療成績・腎障害回避の両面で支持が強まり、E. faecalis IEの標準レジメンとして明確に位置づけられました。
ダプトマイシン高用量(10〜12 mg/kg/日)は、VRE(バンコマイシン耐性腸球菌)IEのサルベージ療法として新規記載されました。推奨レベルはClass IIb、保険適用外であることも明記されています。VRE血流感染の治療選択肢が限られる日本の状況で、現場が混乱しないよう踏み込んだ記載になっています。
部分経口療法(POET)の射程と限界
POET試験(Iversenら、NEJM 2019)は、左心系IE成人400例を対象に、IV治療を10日以上受けた臨床的に安定した症例を「IV継続」と「経口スイッチ」に無作為割付し、6か月の複合アウトカム(全死亡・予期せぬ心臓手術・塞栓イベント・原因菌再燃)で経口群9.0% vs IV群12.1%(非劣性、P=0.40)を示しました。5年の長期追跡でも安全性は維持されています。
この結果を受けて、ESC 2023は条件付きでOPAT・経口スイッチをクラスIIaで推奨しました。
一方、JCS 2026はPOETや「部分経口療法」を主改訂点として前面に据えてはおらず、OPATや長期内服は主にデバイス抜去不能例などの長期抑制療法の文脈で扱われています。感染症専門医の立場としては、国内でPOETを具体的に組む場合はESC 2023のクラスIIa推奨を参照し、JCS 2026本体がこの領域を主改訂としていないことを踏まえた慎重な運用が必要です。
適用には厳格な条件があります。POET原著の登録条件と、ESC 2023および日本での運用を踏まえた実装上の条件は、分けて捉えたほうが正確です。
POET原著の登録条件:
- 原因菌が viridans streptococci、E. faecalis、S. aureus、coagulase-negative staphylococci のいずれか
- 左心系IE
- IV治療10日以上で臨床的に安定している
実装上の条件(ESC 2023の条件付き推奨や国内運用を加味したもの):
- TEEによるフォローが可能
- 高バイオアベイラビリティの経口抗菌薬2剤を併用で組める
- 外来でのフォロー体制が整っている
これらを満たさない症例への一般化は危険で、S. aureus菌血症を伴う不安定例、膿瘍形成例、服薬不遵守が予想される例、吸収不良が懸念される例では、IV継続が安全側の選択になります。
外科が変わった:救済策から前倒し介入へ
IEの外科紹介は、感染症医が最も判断を問われる局面です。ESC 2023と整合的に、JCS 2026でも外科介入をより早い段階で検討する視点が強まり、外科を「救済策」ではなく「転帰改善のための前倒し介入」として捉え直す流れが前面に出ました。
実臨床では、Endocarditis Team(心臓血管外科・循環器内科・感染症科を中心とした多職種合同チーム)が機能している施設と機能していない施設の差は、手術の可否そのものではなく紹介のタイミングに表れます。持続菌血症や疣腫増大を確認してから相談ルートを探し始める施設では、どうしても初動が遅れがちです。感染症科・循環器内科・心臓血管外科のコミュニケーション回路を平時から確立しておくことが、個別症例の判断以前の基盤になります。
外科適応の3本柱とタイミング
外科適応の柱は従来通り3つ、すなわち心不全・コントロール不能感染・塞栓予防で維持されており、これに加えて中枢神経合併症への対応も詳細化されました。timing分類も明確になり、ESC 2023は手術タイミングをemergency(24時間以内)・urgent(3〜5日以内)・非urgent(同一入院中)に整理し、JCS 2026もこれに準じています。心不全を伴う重度弁逆流や穿孔は emergency、コントロール不能感染(持続菌血症、膿瘍形成、弁輪周囲進展)は urgent、塞栓予防目的は非urgentというのが基本枠です。
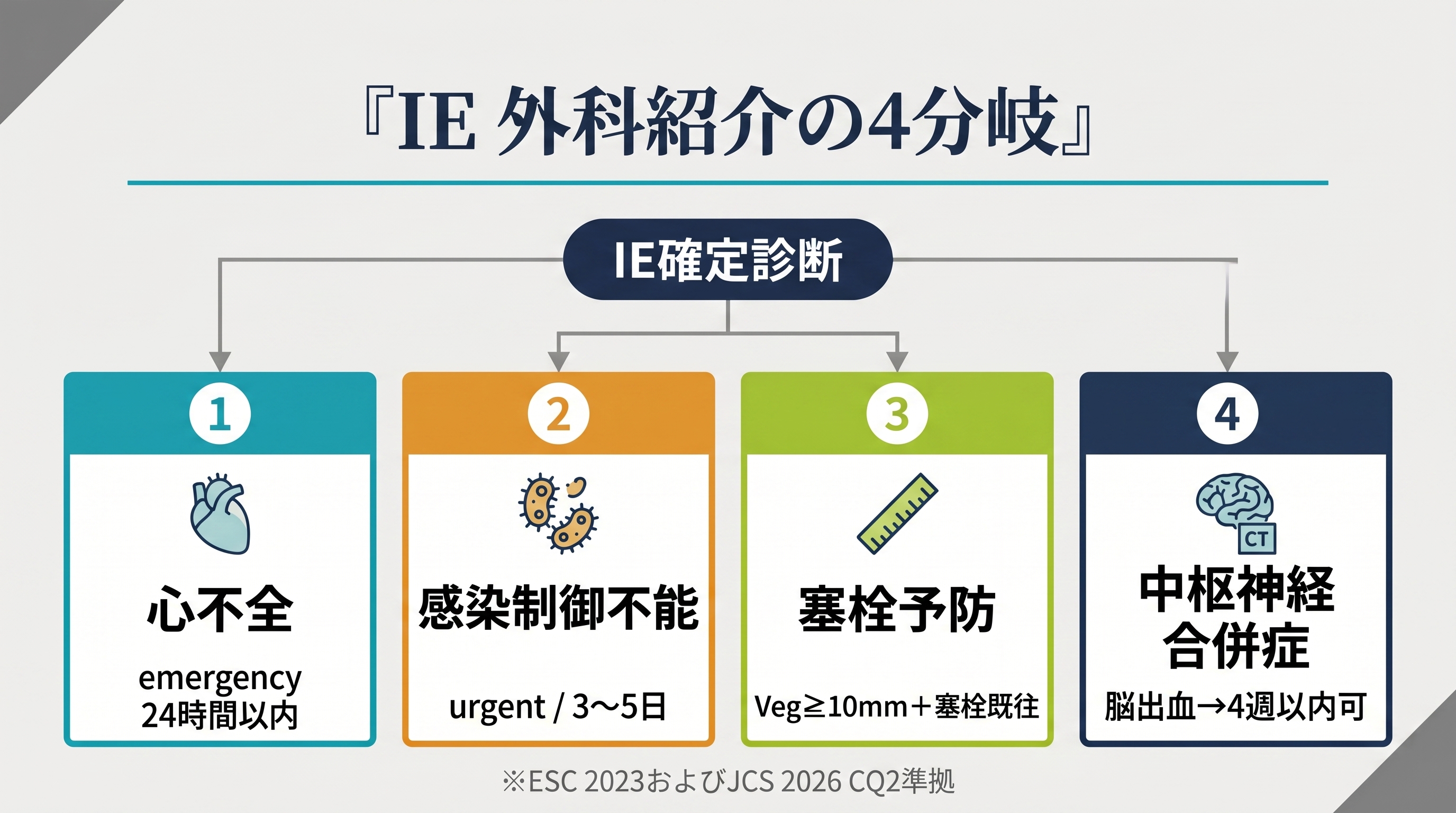
塞栓予防の閾値は大きな論点です。Kangらが2012年にNEJMで報告したEASE試験(韓国、76例)は、左心系・重度弁病変・大きな疣腫(>15 mm)の症例を対象に、「早期手術(48時間以内)」と「従来治療」に無作為割付し、6週間の院内死亡・塞栓イベント複合で早期手術群3% vs 従来群23%(HR 0.10, P=0.03)という明確な差を示しました。2016年の長期追跡でも全死亡と塞栓イベントの複合転帰の低下は維持されています。
EASE自体の対象は大きな疣腫例であり、現行の ESC 2023 が採用している「疣腫≥10mm」基準とは登録条件のサイズがやや異なる点に注意が必要です。ESC 2023は、EASE とその後の観察研究の蓄積を受けて「適切な抗菌薬治療後も塞栓が再発した残存疣腫≥10mm」または「疣腫≥10mmかつ他の手術適応(重度弁逆流・コントロール不能感染)を伴う症例」をClass Iに位置づけています。ただし孤立性の large vegetation 単独を一律 Class I としているわけではなく、適応の個別判断は残ります。
中枢神経合併症後の手術:JCS 2026の転換点
脳梗塞・脳出血合併IEに対する手術タイミングは、JCS 2026のCQ2で正面から扱われた領域です。旧来は脳出血後は一律に待機(ESC・AHAもいずれも「最低4週間延期」を推奨)とされてきましたが、JCS 2026は方針を柔軟化しました。CQ2ステートメントは「適応があれば4週間以内に手術を行ってもよい(推奨の強さ2=弱い推奨、エビデンスC)」で、本文は「1か月以内の早期手術は、明確に推奨するものではないが、禁忌ともいえない」と整理しています。観察研究メタ解析では院内死亡・再出血・神経学的悪化のいずれにも有意差はなく、「救命を要する症例(心不全合併例・弁周囲合併症例)では早期手術の選択肢を閉じない」方針です。
実務上は、神経学的に重症でなく画像上で出血拡大を認めない症例では早期手術の余地を残し、出血拡大例では原則待機、という個別判断になります。
脳梗塞合併例については、治療手技ごとに推奨が細分化されました。主幹動脈閉塞による虚血性脳塞栓症例に対して、血栓回収療法は「速やかに実施を考慮してもよい」(Class IIb C)と新規に記載された一方、経静脈的血栓溶解療法は「推奨されない」(Class III No benefit B)と位置づけられています。「中枢神経合併症があるから手術を諦める、または一律に遅らせる」という反射的判断ではなく、合併症の種類と治療選択肢を個別に評価する姿勢が求められます。
感染症医のマインドセットとしては、「治療継続で様子を見たい」という姿勢が不利益を生む局面があることを意識する時期に来ています。Endocarditis Teamでの意思決定が、個人のバイアスを相殺する仕組みとして機能します。
予防が変わった:歯科処置と高リスク群の再整理
IE予防抗菌薬の適応は、2000年代後半に大幅に縮小されて以降、基本的な枠組みは維持されつつ、個別レジメンの見直しが続いています。
高リスク群 × 高リスク処置の二条件
現行の国際コンセンサスでは、予防抗菌薬は高リスクの心疾患を持つ患者が高リスクの処置を受ける場合に限定されます。AHA 2021 update と ESC 2023 は以下を高リスク心疾患として挙げています。
- 人工弁(機械弁・生体弁・TAVI弁を含む)
- 弁修復に用いた人工物(ring・クリップ等)
- 既往IE
- 未修復チアノーゼ性先天性心疾患または修復後6か月以内
- 弁逆流を伴う心移植後患者
歯科処置のうち予防対象となるのは、歯肉・歯根尖周囲組織の操作を伴うもの、粘膜穿孔を伴うものです。AHA 2021 updateの重要な変更として、クリンダマイシンが予防薬推奨から削除されました(Clostridioides difficile 感染リスクが便益を上回るとの判断)。代替はアモキシシリン、ペニシリンアレルギー時はセファレキシン(非即時型)またはアジスロマイシン・ドキシサイクリンです。
AHA/ESCとJCS 2026のズレ:3層分類
AHA 2021・ESC 2023は歯科以外の多くの処置(通常の消化管内視鏡・膀胱鏡・経直腸超音波等)について routine な予防抗菌薬を非推奨としています。一方JCS 2026は層別化が細かく、以下の3層で整理されています。
| 推奨クラス | 処置例 | 対応 |
|---|---|---|
| IIa C | 観血的手技(膿瘍ドレナージ・感染巣への内視鏡検査治療)、経尿道的前立腺切除術(TUR-P、特に人工弁症例) | 予防抗菌薬投与を考慮してもよい。高度リスク群には予防抗菌薬投与を行う |
| IIb C | 上部・下部消化管内視鏡(生検・ポリープ切除含む)、食道狭窄拡張、尿道拡張術、経膣分娩、心臓カテーテル検査、気管支鏡、皮膚切開(特にアトピー性皮膚炎症例)、骨髄穿刺 等 | 高度リスク群に対して予防抗菌薬投与を考慮してもよい |
| III No benefit | 歯科の非感染部位浸潤麻酔・歯科矯正・抜髄、尿道カテーテル挿入、経尿道的膀胱鏡、中心静脈カテーテル挿入、経食道心エコー 等 | 予防抗菌薬投与は推奨されない |
国際ガイドラインの「歯科以外は原則不要」をそのまま日本の臨床に当てはめるとズレが生じるため、人工弁・既往IEなどの高リスク群では処置前にJCS 2026の該当表を確認する運用が安全です。
歯科処置予防のエビデンス基盤
高リスク群への歯科予防を維持する根拠としては、Tubianaら(BMJ 2017)のフランス全国コホート・症例クロスオーバー研究がよく引かれます。人工弁保有者での侵襲的歯科処置と口腔連鎖球菌IEの関連が観察的に支持されており、ランダム化試験ではないものの、国際的合意の実地的な基盤になっています。
患者説明の場面では、低〜中リスク心疾患(弁膜症一般など)の患者に対する「弁疾患があるから歯科の前に抗生剤」という過剰な予防投与が残っていないかを点検する価値があります。不要な予防投与は耐性菌選択圧を増やし、個人にとっても便益が薄いためです。
JCS 2026を読む3つの視点
JCS 2026を実臨床に落とし込む際、感染症医が持つべき視座は3つです。
第1に、診断はエコーと血液培養だけで完結しません。人工弁・CIED・TAVIなどの特殊病態では、術中直視、心臓CT、FDG-PET/CTがMajor criterionに加わりました。2023 Duke-ISCVID基準で「possible」に留まる症例を「definite」へ引き上げる手段は、旧基準より遥かに多様化しています。核医学科・放射線診断科と事前にプロトコルを合意しておけば、個々の症例での時間損失は避けられます。
第2に、抗菌薬レジメンが骨格から再整理されました。主改訂点は4つです。AMG併用の位置づけ再評価、MSSAへのCTRX単独の後退、腸球菌ABPC+CTRXのClass I格上げ、DAP高用量のVREサルベージ新規記載。一方でPOETの部分経口療法はESC 2023のClass IIa推奨に留まり、JCS 2026では前景化していません。不安定例や膿瘍形成例、服薬や吸収が担保できない例への一般化は禁物で、国内実装にはTEEフォロー・高バイオアベイラビリティの経口2剤・外来フォロー体制が揃った選別運用が前提となります。
第3に、手術は救済策ではなく前倒し介入です。心不全到達前の外科紹介、疣腫≥10mmに塞栓既往または他の手術適応が併存する症例でのClass I相当の外科検討、脳出血合併例でも救命を要する症例では早期手術の選択肢を閉じないこと。この3点のマインドセット転換が感染症医にも求められます。「もう少し抗菌薬で粘りたい」という判断の遅延が、結果として転帰を悪化させる局面は少なくありません。Endocarditis Team(心臓血管外科、循環器内科、感染症科、微生物検査、画像診断、歯科、脳神経内科)での意思決定プロセスが、個人のバイアスを相殺する装置として機能します。
IEは「抗菌薬だけで治す病気」ではなく、「内科・外科・画像・微生物の合同戦」です。抗菌薬の選択を丁寧に積み上げても外科紹介のタイミングが遅れれば転帰は好転しませんし、外科適応を早く議論できる施設でもレジメンがJCS 2026の推奨表に沿っていなければ再発や耐性化を招きます。感染症医の役割はレジメンの各論を追うだけでなく、Endocarditis Teamのハブとして外科紹介の遅延を生まない判断軸を持つことに変わってきています。
目の前の一例ごとに、S. aureus菌血症を見たら疣腫を探し、疣腫を見たら外科に声をかけ、歯科処置を控える患者にはJCS 2026の3層表を開く。その積み重ねが、次のIEを防ぎ、次の改訂を支えるエビデンスを生んでいきます。
関連記事
抗菌薬選択・薬剤耐性菌の文脈で本記事と関連する解説です。
-
抗生物質が効かない——薬剤耐性菌の現実と、私たちにできること
AMRの全体像とアクションプラン2023-2027。IEの起因菌で問題化するMRSA・VRE・AmpCを位置づける総論。 -
AmpC産生菌の治療戦略——IDSA 2024を5軸で読み解く
IE起因菌としては稀だが、感染源不明菌血症やデバイス感染で鑑別に上がる場合のレジメン選択(医療従事者向け)。 -
膀胱炎の薬が効かない時代 — 知っておきたいリスクと対策
尿路由来腸球菌・連鎖球菌菌血症からのIE移行の前段として、市中UTIの抗菌薬選択を整理。
参考文献
-
日本循環器学会. 2026年改訂版 感染性心内膜炎診療ガイドライン(JCS 2026). 2026年3月20日発行. https://www.j-circ.or.jp/cms/wp-content/uploads/2026/03/JCS2026_Izumi.pdf
-
Delgado V, Ajmone Marsan N, de Waha S, et al. 2023 ESC Guidelines for the management of endocarditis: Developed by the task force on the management of endocarditis of the European Society of Cardiology (ESC) Endorsed by the European Association for Cardio-Thoracic Surgery (EACTS) and the European Association of Nuclear Medicine (EANM). Eur Heart J. 2023;44(39):3948-4042. doi:10.1093/eurheartj/ehad193
-
Fowler VG, Durack DT, Selton-Suty C, et al. The 2023 Duke-International Society for Cardiovascular Infectious Diseases Criteria for Infective Endocarditis: Updating the Modified Duke Criteria. Clin Infect Dis. 2023;77(4):518-526. doi:10.1093/cid/ciad271
-
Iversen K, Ihlemann N, Gill SU, et al. Partial Oral versus Intravenous Antibiotic Treatment of Endocarditis. N Engl J Med. 2019;380(5):415-424. doi:10.1056/NEJMoa1808312
-
Kang DH, Kim YJ, Kim SH, et al. Early surgery versus conventional treatment for infective endocarditis. N Engl J Med. 2012;366(26):2466-2473. doi:10.1056/NEJMoa1112843
-
Saby L, Laas O, Habib G, et al. Positron emission tomography/computed tomography for diagnosis of prosthetic valve endocarditis: increased valvular 18F-fluorodeoxyglucose uptake as a novel major criterion. J Am Coll Cardiol. 2013;61(23):2374-2382. doi:10.1016/j.jacc.2013.01.092
-
Tubiana S, Blotière PO, Hoen B, et al. Dental procedures, antibiotic prophylaxis, and endocarditis among people with prosthetic heart valves: nationwide population based cohort and a case crossover study. BMJ. 2017;358:j3776. doi:10.1136/bmj.j3776
-
Tong SYC, Lye DC, Yahav D, et al. Effect of Vancomycin or Daptomycin With vs Without an Antistaphylococcal β-Lactam on Mortality, Bacteremia, Relapse, or Treatment Failure in Patients With MRSA Bacteremia: A Randomized Clinical Trial. JAMA. 2020;323(6):527-537. doi:10.1001/jama.2020.0103
よくある質問
JCS 2026で最も大きな変更点はどこですか?
MSSAに対するセフトリアキソンの位置づけはどう再評価されましたか?
POET(部分経口療法)は日本で実施できますか?
脳出血合併IEの手術タイミングはどう変わりましたか?
その他シリーズで読む
同じシリーズの他の記事です。気になるところから読み進めてみてください。
- コロナ後遺症(Long COVID)2026年の最新知見——原因・治療・最新研究まで
確認感染者の約36%が経験するとされるコロナ後遺症。2026年時点の定義・有力な病態仮説・治療の最前線・日本での受診先を感染症専門医が整理。
