デング熱後のしびれ・脱力に注意 — ギランバレー症候群リスク16.75倍(NEJM 2026)
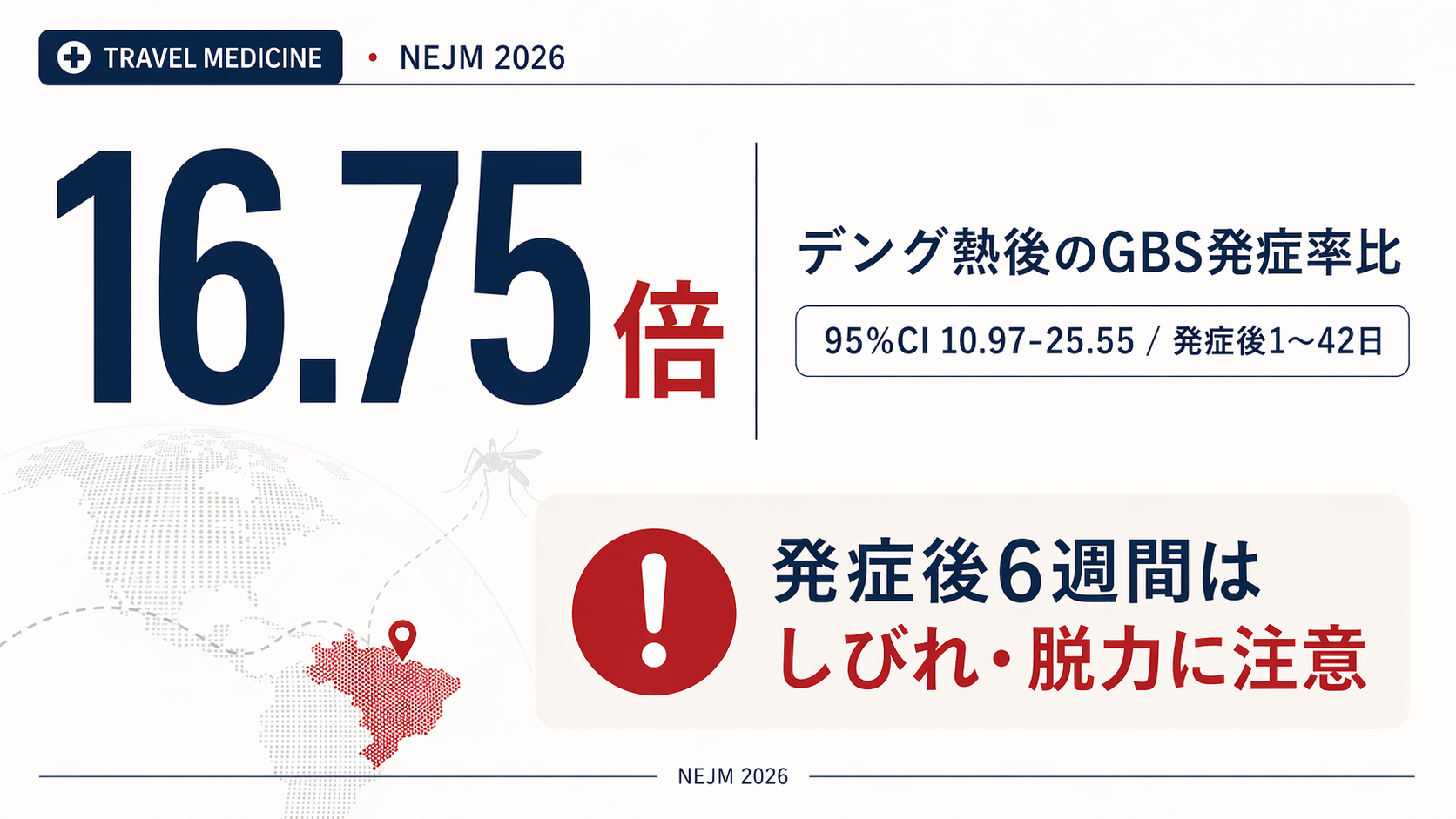
2026年4月中旬、ニューイングランド・ジャーナル・オブ・メディシン(NEJM)に、デング熱と神経合併症の関係を変える可能性のある論文が掲載されました。ブラジル全国の医療データを連結した大規模解析で、デング熱発症後1〜42日のあいだに、ギランバレー症候群(GBS)の発症率が普段の16.75倍に跳ね上がることが示されたのです。
東南アジアや中南米への渡航者にとって、デング熱は今や身近な感染症のひとつです。日本でも2014年以降、多い年には400例超のデング熱届出が記録されており、輸入マラリアを年によって大きく上回っています(年次変動あり)。「熱が下がれば終わり」と思っていた旅行後のだるさや神経症状が、稀ではあるが重大な合併症のサインかもしれない、という認識を更新する必要が出てきました。
この記事のポイント
まず覚えておくべき3点
第一に、デング熱が流行している地域——タイ、ベトナム、フィリピン、インドネシア、インド、ブラジルなど——に出かけるなら、蚊対策を昼間から徹底してください。デング熱を媒介するネッタイシマカ(Aedes aegypti)は日中に活動する蚊で、朝夕にしか刺されない他の蚊とは対策の時間帯が違います。日中の外出時も忌避剤と長袖で刺されないことが第一です。
第二に、デング熱と診断された人は、デング発症日(熱が出た日)を起点に約6週間(NEJM論文のリスク期間1〜42日に相当)は、手足のしびれ・脱力・歩きにくさを観察してください。この期間を過ぎれば、GBSの発症率はほぼ普段のレベルに戻ります。
なお、流行地から帰っただけでデング熱と診断されていない人は、この6週間観察の対象ではありません。ただし帰国後に発熱した場合はデング熱を疑い、発熱日を記録しておいてください。後日神経症状が出た場合、デング発症日が医師にとって重要な情報になります。
第三に、症状が出たら早めに医療機関を受診し、「最近デング熱にかかった」「流行地から帰国した」ことを必ず医師に伝えてください。ギランバレー症候群の治療は、発症から早いほど効果が高いことが知られています。
ブラジル全国データ解析が示したもの
今回の2026年NEJM論文は、ブラジル全国の医療データ(入院記録・デング熱の届け出・死亡記録)をつなぎ合わせて行った研究です。使われた手法は「自己対照症例研究(Self-Controlled Case Series, SCCS)」という、少し難しそうに聞こえる名前のデザインですが、発想はシンプルです。
比較のために他の人を連れてくるのではなく、同じ患者さんの中で「デング熱にかかったあとの期間」と「かかる前や時間が経ったあとの期間」を比べます。こうすることで、年齢・性別・もともと持っている病気といった、人ごとに違う条件の影響を受けにくくなります。ただし、食中毒やインフルエンザが流行る季節の違いのように、時間とともに変わる要因は、別に考える必要があります。
2023〜2024年のブラジル全国データで、ギランバレー症候群による入院は合計5,055件ありました。そのうち、検査でデング熱が確認されていた人は147例。さらに、その147例のうち89例は、デング発症から1〜42日(NEJM論文がリスク期間と定めた範囲)の間にGBSを発症していました。
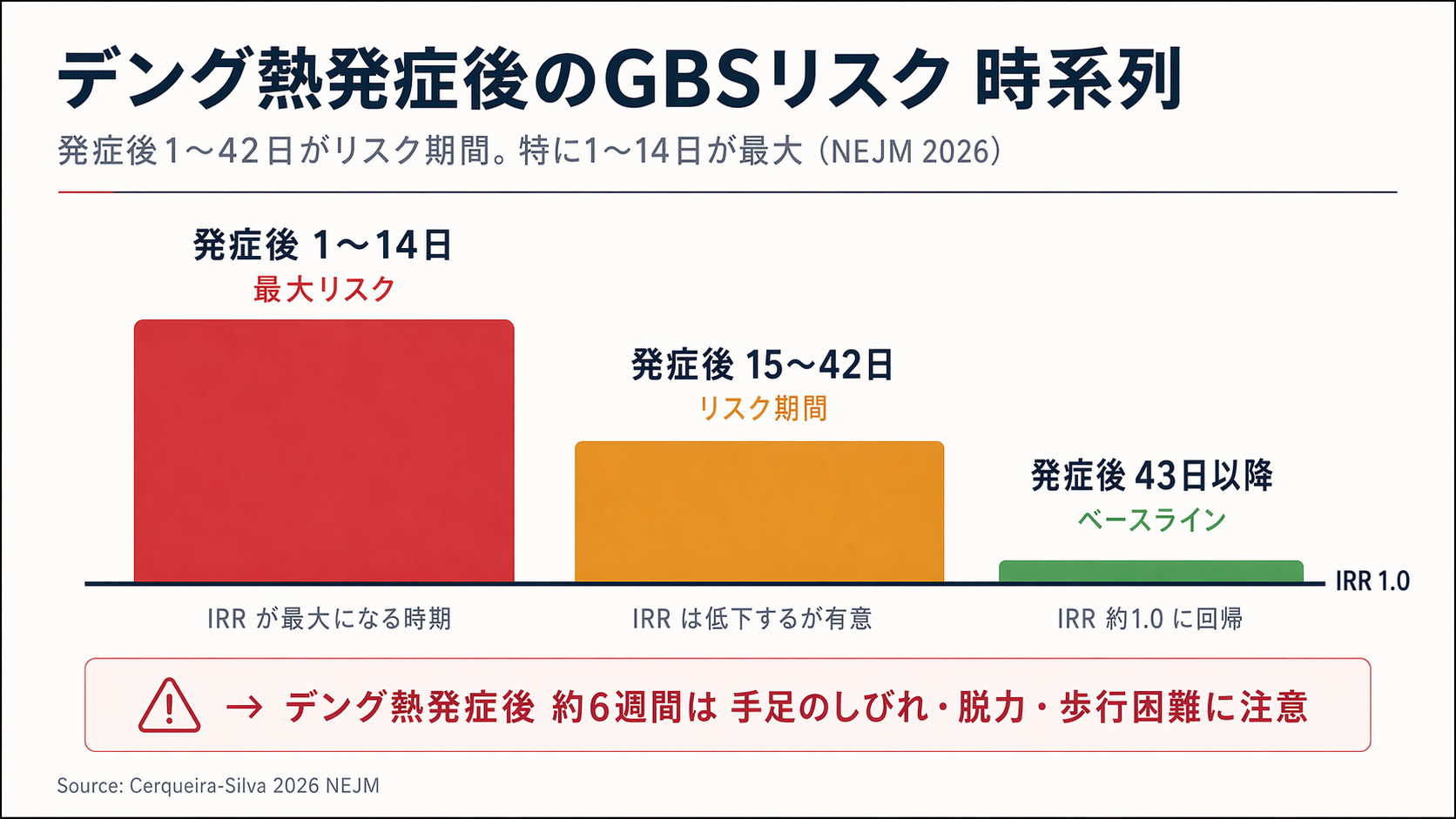
リスクは発症後最初の2週間で最も高く、42日を過ぎると普段のレベルに戻りました。これまでも症例報告レベルではデング後のGBSは散発的に報告されていましたが、2025年BMC Infectious Diseasesの系統的レビューで報告された56例も含め、個別症例の寄せ集めが中心でした。ブラジル全国の連結データで、これまで曖昧だった「どれくらいリスクが上がるのか」という数字の輪郭を描いた点に、この論文の意義があります。
ただし、この研究の解釈には限界もあります。
- 入院GBSを対象とした観察研究であり、軽症例の把握は限定的な可能性がある
- ブラジル住民のデータで、日本人渡航者集団への外的妥当性は別途検討を要する
- 流行する血清型の差が結果に影響する可能性がある
これらを踏まえたうえで読む必要があります。
GBSトリガーの中での位置づけ
ギランバレー症候群は、感染の後に自分の免疫が末梢神経を攻撃してしまう自己免疫性の神経疾患で、年間10万人あたり1〜2人が発症する稀な病気です。代表的な「引き金」として知られていたのは、以下の3つでした。
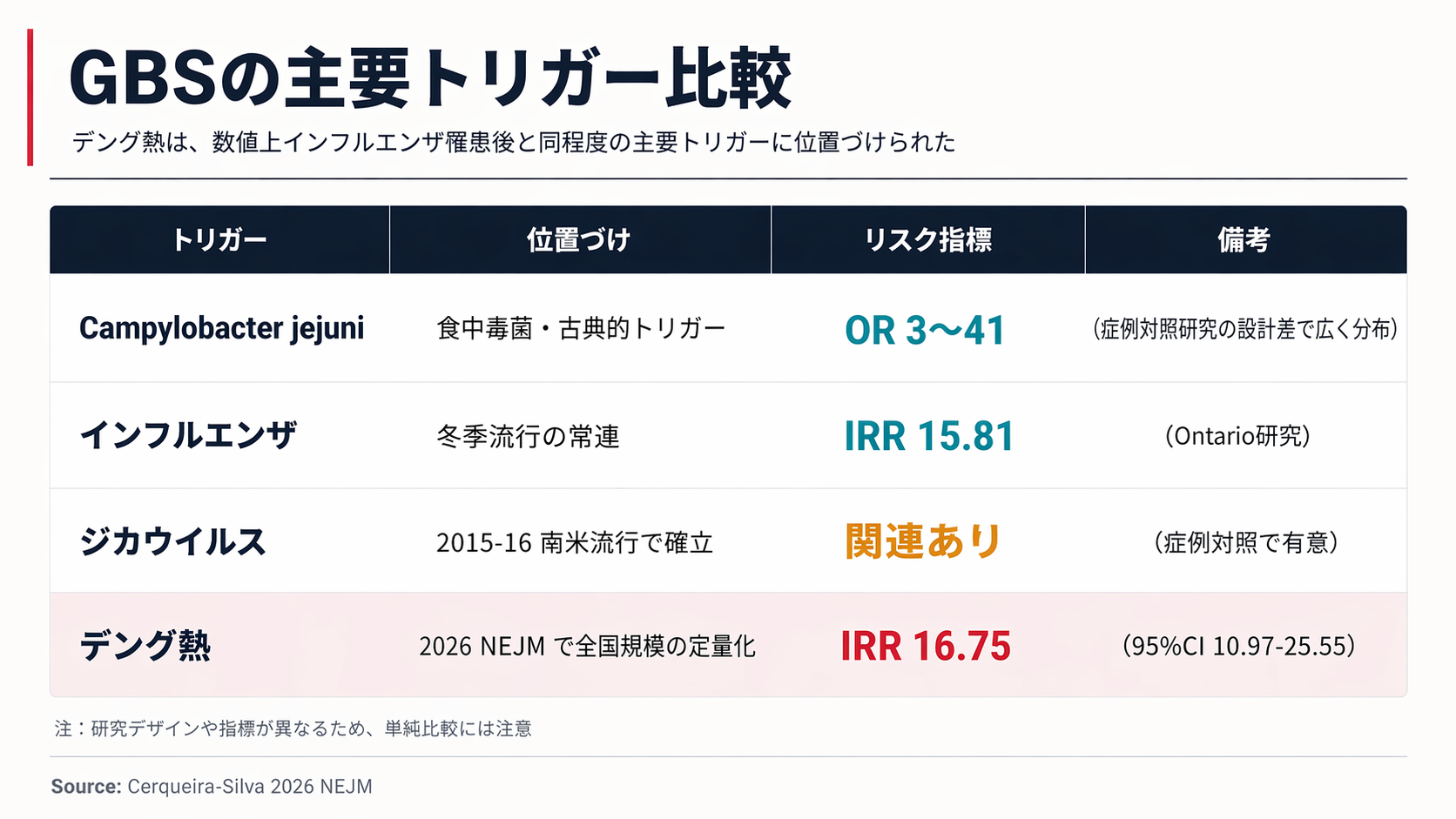
- カンピロバクター属(Campylobacter jejuni、食中毒菌):オッズ比3〜41(症例対照研究の設計差で推定値が広く分布)
- インフルエンザウイルス:発症率比15.81(95%CI 10.28-24.32、Kwong et al. 2013年Lancet Infect Dis、Ontario自己対照研究)
- ジカウイルス:2015〜2016年の中南米流行で確立。2020年のPLOS Neglected Tropical Diseasesに掲載されたメキシコの症例対照研究では、ジカとデングは関連あり、チクングニアは関連なしと報告されました
今回の報告でデング熱の発症率比16.75が加わり、数値としてはインフルエンザと近い水準の相対リスクを持つことが示されました。米国ミネソタ大学のCIDRAP(感染症研究政策センター)も「インフルエンザに匹敵する程度のリスク」と解説しています。
ただし、並べた数値は由来する研究・母集団・統計指標が異なるため、厳密な順位づけや単純な比較には注意が必要です。カンピロバクターの値はオッズ比(OR:症例対照研究で使われる指標)、インフルエンザとデングは発症率比(IRR:時間あたりの発症頻度を比較する指標)で、計算のしかたも比較の土台も違います。また比較はあくまで相対リスクの話で、個人が負う絶対リスクは低い水準であることも強調しておきたい点です。この比較は、「過度に恐れるべきか、無視していいか」を判断する材料として位置づけてください。
渡航者のリスクをどう見積もるか
デング熱にかかった人100万人あたり35.5例のGBSが超過発症する計算で、デング熱に罹患した人一人あたりの絶対リスクは0.0036%程度です。ただし、このリスクの前提となる「そもそもデング熱にかかる確率」が、渡航先・季節・滞在期間で大きく変動します。
GeoSentinel監視ネットワーク(世界33か国の渡航医学施設が参加)の2024年Journal of Travel Medicine論文では、2007〜2022年の15年間で5,958例の輸入デング症例が記録され、地域によってはマラリアより高頻度の帰国後発熱原因となっていることが報告されています。
自分のリスクを見積もるうえで、次の因子を一度点検してみてください。
- 渡航先の流行度:東南アジアの都市部、カリブ海、中南米、インド亜大陸は高い
- 季節:雨季の直後(アジアなら5〜10月ごろ)は蚊が多く、罹患率が上がる
- 滞在期間:長期ほど累積リスクが増す。数日の出張と数か月の留学ではまったく別物
- 宿泊環境:網戸・エアコンありのホテルと、屋外テント泊では刺される頻度が違う
- 過去のデング感染歴:別の血清型での再感染は、重症化リスク(抗体依存性感染増強、ADE)に影響する
これらを足し合わせて「自分のリスクは高い方向」と判断される場合は、予防策にも強めに踏み込む判断が成立します。一律に怖がる必要もなく、一律に無視していい話でもない、という粒度です。
蚊対策が予防の主軸
予防の主軸は、渡航者にとって蚊対策です。
ネッタイシマカは日中に活動する昼行性の蚊で、朝夕にしか刺されない他のマラリア媒介蚊と対策の時間帯が異なります。
具体的には、DEET(ディート)またはイカリジン配合の忌避剤を日中から塗り続けること、長袖長ズボンの着用、宿舎での網戸・エアコン・蚊帳の確認が基本になります。
米国CDCのYellow Book 2026も、米国人旅行者に対する推奨ワクチンは現時点で置かず、蚊対策を中心に据えています。
なお、DEET・イカリジン配合の忌避剤は、日本国内のマダニ媒介感染症の予防でも同じ基本装備になります。GW前後の国内アウトドアでの備えは「マダニ感染症SFTS、千葉県で飼い猫が初確認 — GW前の予防と受診の目安」で整理しています。
デングワクチン(Qdenga)の位置づけ
ワクチンの選択肢として、現在国際的に使われている主な製剤は「Qdenga」(一般名TAK-003、タケダ製)です。2019年NEJM掲載のTIDES試験(4〜16歳の流行地小児約20,000人対象)で発症予防80.2%を示し、2024年Lancet Global Healthに掲載された長期解析では、5年累積で検査確定デング予防61.2%、入院予防84.1%を維持しています。
ただし、これらの有効性データは主に流行地の小児・思春期集団から得られたもので、渡航者である成人への外的妥当性は別途の検討を要します。
世界40か国超で承認されていますが、日本では未承認で、日本企業が開発したワクチンである一方、日本国内ではまだ使えないというねじれがあります。日本の渡航医療提供者154人を対象とした2025年の調査では、75%が長期旅行者には推奨する意向を示しました。
渡航者にとってのワクチン判断には、いくつか押さえておきたい実務ポイントがあります。
第一に、Qdengaは3か月間隔の2回接種が基本設計です。出発直前に検討を始めても、出発までに2回完了するのは実務上難しいことが少なくありません。旅行者での具体的な接種計画は、渡航期間や渡航先、現地での継続接種の可否を含めて個別に判断が必要です。
第二に、既感染歴の解釈です。前世代のデングワクチン「Dengvaxia」について、2018年NEJMに掲載された解析では、事前のデング感染歴がない人に接種すると、その後に自然感染した際に重症化・入院リスクが上がる(ハザード比1.75、95%CI 1.14-2.70)と示されました。これはDengvaxia特有の問題ですが、デングワクチン一般に「既感染歴の確認が判断を左右する」という慎重姿勢を広げた歴史的経緯があります。
Qdenga自体は2024年WHOポジションペーパーで、高伝播地域の6〜16歳を対象にした公衆衛生プログラムでの使用が推奨されており、流行地の小児集団と渡航者への応用では判断の枠組みが異なります。
スイスの渡航医学ガイダンスをまとめた2024年Swiss Medical Weeklyの整理では、既感染が確認されているか強く示唆される反復・長期渡航者では検討しうる一方、既感染不明の初回短期旅行者には勧めにくい、とまとめられています。海外接種の選択肢も含めて、渡航外来のある医療機関で出発2〜3か月前には一度相談してみてください。ほかの渡航ワクチンと合わせた判断は、「髄膜炎菌ワクチンの日本での現状」も参考になります。
「熱が下がれば終わり」を更新する
「デング熱は熱が下がれば終わり」という認識は、今回のNEJM論文を契機に少し更新しておいたほうがいい、というのが感染症診療の側から見た1つの読み方です。稀ではあるが見逃してはいけない神経合併症がある、という1点だけでも、臨床判断は変わります。
近年、感染後に続く体調不良を「感染後慢性疾患」(Infection-Associated Chronic Condition, IACC)として統合的に捉える見方が広がってきました。関連する話題は「Long COVIDはなぜ終わっていないのか」でも整理しています。急性期を乗り切ったあとのフォローアップ窓を、熱帯感染症にも広げて考える。今回の論文は、その方向への小さな、しかし明確な一歩だと受け止めています。
帰国後の発熱そのものを受診タイミングでどう判断するかは、別記事「GW帰国後の発熱、受診の目安と気になるサイン|渡航先別トリアージガイド」で整理しています。
デング熱は「熱が下がれば終わりの熱帯感染症」ではなく、「発症から6週間は神経症状を見守る感染症」に位置づけが変わってきています。絶対リスクが低いことを理由に見送るのではなく、絶対リスクが低いからこそ見逃さない、という姿勢が一次医療と渡航医療の接点で求められるようになります。
目の前の旅行者に、出発前には蚊対策を、帰国後に発熱したら発熱日の記録を、6週間のあいだ神経症状が出たら受診時にデング発症日を共有することを、一つずつ伝えていく。その積み重ねが、稀な神経合併症を取りこぼさない診療の厚みになっていきます。
参考文献
-
Cerqueira-Silva T, Paixão E, et al. Risk of Guillain-Barré Syndrome after Laboratory-Confirmed Dengue Infection. N Engl J Med. 2026. doi:10.1056/NEJMc2519008
-
Effiong MG, Yakubu AO, Lawal FI, et al. Dengue virus infection and Guillain-Barré syndrome: a systematic review of clinical characteristics, outcomes, and predictors of severity. BMC Infect Dis. 2026;26:133. doi:10.1186/s12879-025-12428-7
-
Garg RK, Mahdi RA, Malhotra HS, et al. Spectrum of Neuromuscular Manifestations in Dengue: A Systematic Review of Case Reports and Case Series. Ann Indian Acad Neurol. 2025;28(6):798-805. PMID: 41370007
-
Grijalva I, Grajales-Muñiz C, González-Bonilla C, et al. Zika and dengue but not chikungunya are associated with Guillain-Barré syndrome in Mexico: A case-control study. PLoS Negl Trop Dis. 2020;14(12):e0008032. doi:10.1371/journal.pntd.0008032
-
Duvignaud A, Stoney RJ, Angelo KM, et al. Epidemiology of travel-associated dengue from 2007 to 2022: A GeoSentinel analysis. J Travel Med. 2024;31(7):taae089. doi:10.1093/jtm/taae089
-
Biswal S, Reynales H, Saez-Llorens X, et al. Efficacy of a Tetravalent Dengue Vaccine in Healthy Children and Adolescents. N Engl J Med. 2019;381(21):2009-2019. doi:10.1056/NEJMoa1903869
-
Tricou V, Yu D, Reynales H, et al. Long-term efficacy and safety of a tetravalent dengue vaccine (TAK-003): 4·5-year results from a phase 3, randomised, double-blind, placebo-controlled trial. Lancet Glob Health. 2024;12(2):e257-e270. doi:10.1016/S2214-109X(23)00522-3
-
Sridhar S, Luedtke A, Langevin E, et al. Effect of Dengue Serostatus on Dengue Vaccine Safety and Efficacy. N Engl J Med. 2018;379(4):327-340. doi:10.1056/NEJMoa1800820
-
Eperon G, Veit O, Antonini P, et al. Vaccination against dengue fever for travellers. Swiss Med Wkly. 2024;154:3858. doi:10.57187/s.3858
-
World Health Organization. Dengue vaccines: WHO position paper, May 2024. Wkly Epidemiol Rec. 2024;99(18):203-224. https://www.who.int/publications/i/item/who-wer-9918-203-224
-
国立健康危機管理研究機構. デング熱(詳細版). https://id-info.jihs.go.jp/infectious-diseases/dengue-fever/detail/index.html(参照日: 2026-04-22)
-
Fukunishi A, Machida M, Fukushima S, et al. Travel medicine providers’ opinions on the dengue vaccine TAK-003 as a travel vaccine and the need for decision-support information and materials before its launch in Japan. Hum Vaccin Immunother. 2025;21(1):2483560. doi:10.1080/21645515.2025.2483560
-
Kwong JC, Vasa PP, Campitelli MA, et al. Risk of Guillain-Barré syndrome after seasonal influenza vaccination and influenza health-care encounters: a self-controlled study. Lancet Infect Dis. 2013;13(9):769-776. doi:10.1016/S1473-3099(13)70104-X
よくある質問
デング熱にかかったら、必ずギランバレー症候群になるのですか?
Qdenga(デング熱ワクチン)は日本で接種できますか?
このNEJM論文は、なぜ今注目されているのですか?
帰国後にしびれや脱力が出たら、すぐ病院に行くべきですか?
デング熱の診断が出ていない場合も、帰国後のしびれは気にすべきですか?
渡航・帰国後シリーズで読む
同じシリーズの他の記事です。気になるところから読み進めてみてください。
- PILLAR GW帰国後の発熱、受診の目安と気になるサイン|渡航先別トリアージガイド
ゴールデンウィーク中・明けに海外から戻った後の発熱、慌てる前に知っておきたい受診の目安があります。マラリア・デング・腸チフス・レプトスピラを潜伏期間と渡航先で整理し、受診のタイミングと受診前のセルフケアを専門医の視点でまとめます。
