「培養検査の結果が出ました。ESBL産生菌です」
外来でこう伝えると、多くの患者さんが不安な表情を浮かべます。聞き慣れない名前、「耐性菌」という響き。「隔離が必要ですか」「家族にうつりますか」と聞かれることも珍しくありません。
結論から言えば、保菌しているだけなら治療の必要はなく、日常生活に制限もいりません。ただし、この菌が実際に感染症を引き起こしたとき、使える薬の選択肢は狭くなります。だからこそ、その正体を知っておく意味があります。
この記事のポイント
ESBL産生菌とは
ESBL(Extended-Spectrum Beta-Lactamase)は、日本語で基質特異性拡張型β-ラクタマーゼと呼ばれる酵素です。ペニシリン系やセフェム系など、日本の外来で広く処方される抗菌薬を分解してしまいます。
わかりやすく言えば、抗菌薬は細菌を攻撃する「弾丸」のようなものですが、ESBLはその弾丸を撃ち落とす「盾」にあたります。この盾を持った細菌には、通常の弾丸が届きません。
この酵素を持つ菌は、大腸菌(Escherichia coli)や肺炎桿菌(Klebsiella pneumoniae)など、腸内細菌目に属する複数の菌種にまたがります。なかでも市中感染で圧倒的に多いのは大腸菌です。大腸菌は私たちの腸に住む常在菌であり、それ自体は有害ではありません。問題は、この常在菌の一部がESBLという「盾」を獲得したことにあります。
「保菌」と「感染」は違う
ここでひとつ、大切な区別を押さえておきます。
- 保菌: ESBL産生菌が腸の中にいるが、症状はない状態
- 感染: ESBL産生菌が尿路や血液など本来いるべきでない場所に入り込み、症状を起こしている状態
保菌であれば、治療は不要です。検査で菌が見つかったこと自体に過度な心配はいりません。問題になるのは、この菌が実際に感染症を引き起こしたとき。そのときに使える薬が限られることが、この菌を「知っておくべき存在」にしているのです。
では、このESBLにはどんな種類があり、どうやって検出するのか。
ESBLの3つの型
それぞれ多数の変異型が報告されていますが、臨床上重要なのは主に以下の3つです。
| 型 | 起源 | 特徴 | 臨床的な位置づけ |
|---|---|---|---|
| TEM型 | TEM-1(1965年、ギリシャ)から派生 | 1980〜90年代に欧米の入院患者で主流。K. pneumoniae 中心。ceftazidimeに耐性を取られやすい | 現在は減少傾向 |
| SHV型 | SHV-1(1972年、K. pneumoniae の染色体性酵素)から派生 | SHV-2(1983年、ドイツ)が初のESBL。TEM型と類似した耐性パターン | TEM型と並ぶ古典的ESBL |
| CTX-M型 | 環境中の Kluyvera 属の染色体遺伝子が起源 | 2000年代以降に世界的に急増。大腸菌中心。ceftazidimeよりもcefotaximeに耐性を示す傾向がある | 現在最も重要。市中感染の主因 |
かつてESBL産生菌は、集中治療室や長期入院の患者から検出される「病院の菌」でした。主役はTEM型やSHV型で、K. pneumoniae が問題の中心でした。
しかし2000年代以降、CTX-M型が世界を一変させます。環境細菌に由来する遺伝子が、挿入配列(ISEcp1など)の力でプラスミドに乗り移り、大腸菌に取り込まれたのが始まりです。プラスミドは細菌間で水平伝達されるため、種を越えて急速に拡散しました。
日本では当初CTX-M-9グループ(CTX-M-14、CTX-M-27)が優位でしたが、近年はCTX-M-15も増加しています。CTX-M-15は他のCTX-M型と比べてセフタジジムへの耐性に結びつきやすく、同じプラスミド上にフルオロキノロン耐性遺伝子やアミノグリコシド修飾酵素遺伝子を同時に搭載していることが多い点が特徴です。ひとつのプラスミドが多剤耐性の「パッケージ」になっている構造が、拡散を加速させています。日本のESBL疫学はCTX-M-27やST131のH30Rサブクローンなども絡み、単純ではありません。
ST131クローンの世界的拡散
CTX-M型ESBLを持つ大腸菌の中で、世界的に注目されているのがST131と呼ばれるクローン(系統)です。血清型O25:H4、phylogenetic group B2に分類されるこの系統は、フルオロキノロン耐性も同時に持つことが多く、世界中の市中尿路感染症から検出されています。日本でもST131はESBL産生大腸菌の主要クローンの一つとして確認されており、市中感染の背景にこの系統の拡散があります。
ESBLの検出
臨床検査室では、大腸菌や肺炎桿菌が第3世代セファロスポリン(セフォタキシム、セフトリアキソンなど)に耐性を示した場合にESBLを疑います。確認試験ではクラブラン酸(β-ラクタマーゼ阻害薬)を加えてMIC(最小発育阻止濃度)が8倍以上低下するかを調べます。「阻害薬で耐性が解除される」のがESBLの特徴です。セファマイシン系(セフメタゾールなど)やカルバペネム系には感受性を保つ点が、他の耐性機序(AmpC、カルバペネマーゼ)との鑑別ポイントになります。
日本でどれくらい広がっているか
厚生労働省の院内感染対策サーベイランス(JANIS)の2023年データです。ここでいう「セフォタキシム耐性」はESBLそのものではありませんが、ESBL産生の良い代理指標として広く使われており、この耐性の背景にはESBLが重要な役割を果たしていると考えられています。
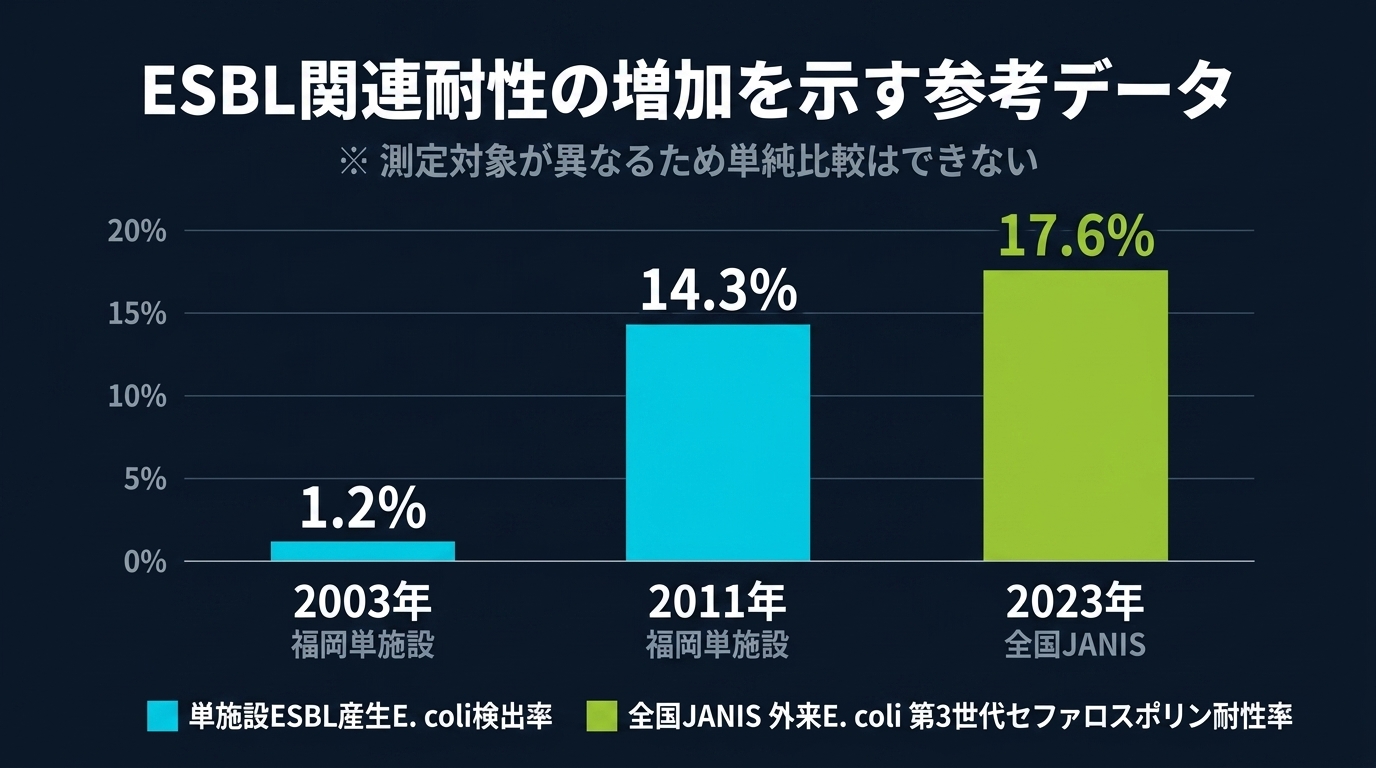
注目すべきは外来の数字です。外来由来の E. coli でこれだけの耐性率が確認されるのは、ESBL産生菌が病院の外にまで浸透していることを示唆しています。
個別施設の報告からは、経時変化がより鮮明に見えてきます。福岡の医療機関では、外来の大腸菌のESBL産生率が2003年の1.2%から2011年には14.3%へ急上昇しました。また、東京の3次医療機関1施設の調査では、ESBL産生菌感染症の約4分の1が市中で発症しており、その多くは直近の抗菌薬使用歴がありませんでした。これらは単施設データであり全国像とは直結しませんが、ESBL産生菌がもはや入院患者だけの問題ではないことを裏づけています。
この傾向は日本に限りません。2025年に発表された25研究・約1万4千人を対象とするメタアナリシスでは、世界の健常人におけるESBL産生大腸菌の腸管保菌率は25.4%と推計されています。日本でも健常人からのESBL産生菌保菌が複数の調査で報告されており、市中での拡大が進んでいることを示しています。
外来で膀胱炎の培養を出すと、月に何例かはESBL産生菌が返ってきます。10年前なら驚いた結果が、今は日常です。それほどこの菌は、身近な存在になっています。
食卓・ペット・海外旅行から広がる耐性菌
ESBL産生菌は病院の中だけで増えているわけではありません。食品、動物、環境、国境を越える人の移動。複数の経路を通じて、私たちの暮らしに入り込んでいます。この全体像を理解するために使われるのが「ワンヘルス(One Health)」の視点です。ヒト・動物・環境は互いにつながっており、耐性菌の問題もその接点から広がっている、という考え方です。
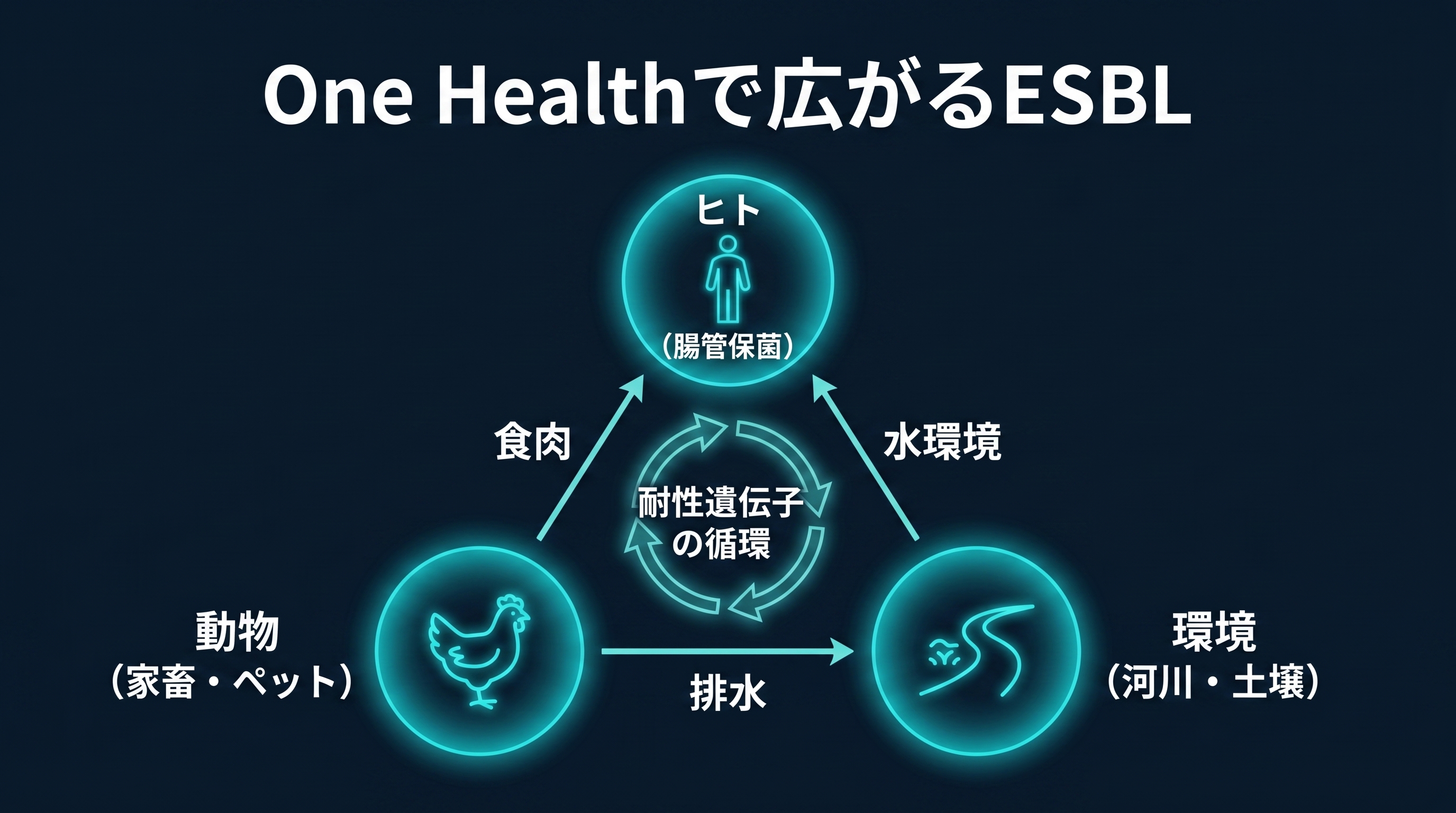
食品からの経路で特に報告が多いのが鶏肉です。国産の鶏肉からもESBL産生大腸菌が高率に検出されたという複数の報告があります。養鶏場では感染症予防のために抗菌薬が使用されることがあり、その環境でESBL産生菌が選択・増殖し、食肉を通じてヒトに届く経路が指摘されています。ペットについても、日本の病気の犬猫から採取された E. coli 株でESBL産生が確認された報告があり、動物との密接な接触が保菌の一因になりうるとされています。
環境中にもこの菌は存在します。日本の河川水からESBL産生大腸菌が検出された報告があり、生活排水や農業排水を介して耐性遺伝子が環境中で循環していることがうかがえます。
海外旅行は、個人レベルでのリスク因子として大規模に研究されています。オランダで約2,000人の旅行者を追跡したCOMBAT研究が、その実態を数字で示しています。
| COMBAT研究の主要結果 | |
|---|---|
| 渡航後の保菌率(全体) | 34.3% |
| 南アジアへの渡航者 | 75.1% |
| 渡航中の抗菌薬使用によるリスク上昇 | 約2.7倍 |
| 12カ月後も保菌が持続 | 11.3% |
なかでもフルオロキノロン系抗菌薬の使用はさらにリスクを高めることが報告されています。保菌の多くは自然に消失しますが、1年後も持続する人や家族への伝播も一定の割合で確認されています。
こう書くと不安が膨らむかもしれませんが、日常の衛生行動でリスクは大きく下がります。鶏肉は中心部まで十分に加熱すれば安全です。ペットとの接触後は手を洗う。渡航先で安易に抗菌薬を買わない。
大切なのは、ESBL産生菌はもう「特別な菌」ではないという認識です。いつ自分が出会ってもおかしくない。だからこそ、もし感染症を起こしたときに治療がどう変わるのかを知っておくことに意味があります。
耐性菌の広がり全体については、「抗生物質が効かない——薬剤耐性菌の現実と、私たちにできること」でも解説しています。
感染したらどうなるか
ESBL産生菌による感染症で最も多いのは膀胱炎や腎盂腎炎などの尿路感染症です。胆道感染症や、それらに起因する菌血症(血液に菌が入り込む状態)の原因にもなります。
すべてが重症になるわけではありません。ただし、以下のような方は注意が必要です。
- 免疫力が低下している(糖尿病、ステロイド使用中、抗がん剤治療中など)
- 高齢で複数の基礎疾患がある
- 尿路カテーテルなど医療デバイスが留置されている
- 繰り返し尿路感染症にかかっている
- 過去に抗菌薬を頻繁に使用した経歴がある
38度以上の発熱、腰や脇腹の痛み、全身のだるさがある場合は、腎盂腎炎や菌血症の可能性があります。早めに医療機関を受診してください。
治療の考え方
ESBL産生菌の治療で最も信頼性が高いのはカルバペネム系抗菌薬です。重症例や菌血症ではこの薬剤が第一選択となることが多く、現時点で最も確実な選択肢です。
なぜ他の薬で代用しにくいのか。2018年に発表されたMERINO試験がその根拠を示しています。ESBL産生菌の菌血症を対象とした初のランダム化比較試験で、ピペラシリン・タゾバクタムとメロペネム(カルバペネム系)を比較しました。
感染部位や重症度でサブグループ解析しても、この傾向は一貫しており、「カルバペネムの代わりに使えるかもしれない」という期待は大きく後退しました。
ただし、この話には続きがあります。後続の解析では、ピペラシリン・タゾバクタムのMICが高い株や、ESBLとOXA-1というβ-ラクタマーゼを併せ持つ株で成績不良が目立ち、非感受性株を除くと群間差は縮小しました。ピペラシリン・タゾバクタムそのものが悪いのではなく、「見かけ上は感受性でも、実際にはMICが高い株」が紛れ込んでいた可能性がある。MERINO試験の結論は、見た目ほど単純ではありません。この点は今後の記事で詳しく取り上げます。
すべてのESBL感染症にカルバペネムが必要なわけでもありません。「尿からESBLが出た」だけで一律にカルバペネムに寄せるのではなく、感染部位・重症度・菌血症の有無・感受性検査の結果で治療戦略を分けることが本筋です。
感染部位と重症度で変わる治療薬選択
| 臨床状況 | 第一選択 | 代替薬(感受性確認が前提) |
|---|---|---|
| 菌血症・重症感染 | カルバペネム系(メロペネムなど) | 原則代替なし(MERINO試験の教訓) |
| 軽症〜中等症の点滴治療(尿路・胆道) | カルバペネム系 | セフメタゾール(セファマイシン系) |
| 経口治療への切替・外来治療 | ST合剤、フルオロキノロン | 感受性に応じて個別判断 |
日本ではセフメタゾール(セファマイシン系)の使用経験が豊富です。ESBL産生大腸菌による感染症、特に尿路由来や比較的安定した症例で有望性を示す観察研究が複数報告されています。ただし、いずれも観察研究が主体であり、重症例への安易な適用は避けるべきです。セファマイシン系はESBLには分解されませんが、AmpC型β-ラクタマーゼには不安定であり、治療中に外膜蛋白の変異を介した耐性化が起きうる点にも注意が必要です。
経口薬では、感受性が確認されたST合剤(スルファメトキサゾール・トリメトプリム)やフルオロキノロンが候補になります。米国感染症学会(IDSA)の2024年ガイダンスでも、腎盂腎炎や複雑性尿路感染に対して感受性確認済みのこれらの使用が示されています。一方、ニトロフラントインやホスホマイシン、アモキシシリン・クラブラン酸は菌血症からの経口切替には推奨されていません。
ここで忘れてはならないのが、カルバペネム系抗菌薬が感染症治療における「最後の切り札」であるという事実です。この薬を多用すれば、カルバペネムにすら耐性を持つ菌(CRE:カルバペネム耐性腸内細菌目細菌)が増えるリスクがあります。必要なときに確実に使い、不要なときには温存する。ESBL時代の感染症診療は、このバランスの上に成り立っています。
尿路感染症全体については、「膀胱炎の薬が効かない時代 — 知っておきたいリスクと対策」で詳しくまとめています。
自分を守るためにできること
ESBL産生菌から身を守るために、特別な装備はいりません。日常の基本を確実に実行することが、最も有効な対策です。
手洗いと衛生管理
ESBL産生菌は、腸管内に保菌した菌が手指や環境を介して広がることがあります。トイレの後、食事の前、生肉を扱った後の石けんと流水による手洗いが最も基本的で有効な対策です。手洗いが難しい場面ではアルコール手指消毒も補助的に使えます。まな板や調理器具は、生肉用と加熱済み食品用で使い分けてください。鶏肉は中心温度75℃以上で確実に加熱すれば、菌は死滅します。
海外渡航時の注意
南アジアや東南アジアなど保菌率の高い地域へ渡航した後は、腸内にESBL産生菌がいる可能性があります。症状がなければ検査は不要ですが、帰国後に尿路感染症を発症した場合は、渡航歴を医師に伝えてください。治療薬の選択に直結する情報です。
渡航先の薬局で抗菌薬を購入して自己判断で服用することは、前述のCOMBAT研究でも保菌の主要リスク因子として挙げられています。下痢が続く場合は、自己判断での服薬を避け、現地の医療機関を受診してください。
培養検査を「答え合わせ」に
ESBL産生菌による感染症では、培養検査なしに最適な治療薬を選ぶことはできません。尿路感染症を繰り返す方、過去にESBL産生菌が見つかったことがある方は、症状が出た段階で早めに培養検査を提出することをお勧めします。
結果は、今回の治療の答え合わせになるだけでなく、次に感染したときの参考資料にもなります。「どの薬が効くか」を一度把握しておくことで、再発時により迅速な対応が可能になります。
保菌しているだけなら治療は不要
検査でESBL産生菌が見つかっても、症状がなければ治療の必要はありません。尿に菌がいるだけで症状がない「無症候性細菌尿」に抗菌薬を使うと、菌を除去できないばかりか、かえって新たな耐性を生む原因になります。「菌がいる」と「治療が必要」はイコールではない。この理解が大切です。
冒頭の場面に戻ります。「ESBL産生菌です」と伝えられた患者さんに、私は続けてこう話します。「保菌しているだけなら治療はいりません。もし感染症を起こしていても、培養結果を見れば最適な薬を選べます」。
ESBL産生菌は、もはや病院の中だけの存在ではなくなりました。食卓に、旅先に、日々の暮らしの中に、この菌は静かに広がっています。それでも、正しく知り、正しく対処すれば、多くの場合は問題なく治療できます。自分の菌を知ること。培養検査を受け、医師と一緒に最善の一手を選ぶこと。その一歩が最も確かな備えです。
関連記事
薬剤耐性菌シリーズとして、以下の記事も合わせてお読みください。
参考文献
-
厚生労働省健康・生活衛生局. 抗微生物薬適正使用の手引き 第四版 薬剤耐性菌感染症の抗菌薬適正使用編. https://www.mhlw.go.jp/content/10900000/001630929.pdf(参照日: 2026-04-17)
-
厚生労働省. 院内感染対策サーベイランス事業(JANIS)検査部門 公開情報 2023年年報. https://janis.mhlw.go.jp/(参照日: 2026-04-17)
-
Paterson DL, Bonomo RA. Extended-spectrum beta-lactamases: a clinical update. Clin Microbiol Rev. 2005;18(4):657-86. doi:10.1128/CMR.18.4.657-686.2005
-
Nicolas-Chanoine MH, et al. Escherichia coli ST131, an intriguing clonal group. Clin Microbiol Rev. 2014;27(3):543-74. doi:10.1128/CMR.00125-13
-
Chong Y, et al. Community spread of extended-spectrum β-lactamase-producing Escherichia coli, Klebsiella pneumoniae and Proteus mirabilis: a long-term study in Japan. J Med Microbiol. 2013;62(Pt 7):1038-43. doi:10.1099/jmm.0.059279-0
-
Ng RWY, et al. Global prevalence of human intestinal carriage of ESBL-producing E. coli during and after the COVID-19 pandemic. JAC Antimicrob Resist. 2025;7(1):dlaf001. doi:10.1093/jacamr/dlaf001
-
Arcilla MS, et al. Import and spread of extended-spectrum β-lactamase-producing Enterobacteriaceae by international travellers (COMBAT study): a prospective, multicentre cohort study. Lancet Infect Dis. 2017;17(1):78-85. doi:10.1016/S1473-3099(16)30319-X
-
Harris PNA, et al. Effect of piperacillin-tazobactam vs meropenem on 30-day mortality for patients with E coli or Klebsiella pneumoniae bloodstream infection and ceftriaxone resistance: a randomized clinical trial. JAMA. 2018;320(10):984-994. doi:10.1001/jama.2018.12163
-
Fukuchi T, et al. Cefmetazole for bacteremia caused by ESBL-producing Enterobacteriaceae comparing with carbapenems. BMC Infect Dis. 2016;16:427. doi:10.1186/s12879-016-1770-1
-
Hayakawa K, et al. Effectiveness of cefmetazole versus meropenem for invasive urinary tract infections caused by extended-spectrum β-lactamase-producing Escherichia coli. Antimicrob Agents Chemother. 2023;67(10):e00510-23. doi:10.1128/aac.00510-23
-
Matsumura Y, et al. Multicenter retrospective study of cefmetazole and flomoxef for treatment of extended-spectrum-β-lactamase-producing Escherichia coli bacteremia. Antimicrob Agents Chemother. 2015;59(9):5107-13. doi:10.1128/AAC.00701-15
-
Tamma PD, et al. Infectious Diseases Society of America 2024 Guidance on the Treatment of Antimicrobial-Resistant Gram-Negative Infections. Clin Infect Dis. 2024;ciae403. doi:10.1093/cid/ciae403
-
西村翔. 基礎から臨床につなぐ 薬剤耐性菌のハナシ(連載第6〜10回, ESBL). J-IDEO(中外医学社). 2018.
-
Hayakawa K, et al. Epidemiology of extended-spectrum beta-lactamase (ESBL) producing Escherichia coli in Japan: Characteristics of community-associated versus healthcare-associated ESBL E. coli. J Infect Chemother. 2017;23(2):117-119. doi:10.1016/j.jiac.2016.08.010
-
Henderson A, et al. Association between minimum inhibitory concentration, beta-lactamase genes and mortality for patients treated with piperacillin/tazobactam or meropenem from the MERINO study. Clin Infect Dis. 2021;73(11):e3842-e3850. doi:10.1093/cid/ciaa1479
-
食品安全委員会. 食中毒予防のポイント. https://www.fsc.go.jp/sonota/shokutyudoku.html(参照日: 2026-04-17)
よくある質問
ESBL産生菌は人にうつりますか?
「ESBL産生菌が出ました」と言われたら隔離が必要ですか?
海外旅行から帰ったらESBLの検査を受けたほうがいいですか?
ESBL産生菌に効く薬はありますか?
鶏肉を食べるとESBL産生菌に感染しますか?
薬剤耐性菌・抗菌薬選択シリーズで読む
同じシリーズの他の記事です。気になるところから読み進めてみてください。
- PILLAR 抗生物質が効かない——薬剤耐性菌の現実と、私たちにできること
2050年までに累計3,900万人が死亡するとも推計される薬剤耐性菌(AMR)。風邪に抗生物質が効かない理由から、家庭でできる耐性菌対策まで専門医がわかりやすく解説。
- AmpC産生菌の治療戦略——IDSA 2024を5軸で読み解く
AmpC産生菌の治療をIDSA 2024を軸に整理。菌種別リスク、セフェピムとP/Tの使い分け、日本の疫学を感染症専門医が解説。
- 膀胱炎の薬が効かない時代 — 知っておきたいリスクと対策
膀胱炎の薬が3割効かない時代。リスク・予防・ESBL耐性菌の問題まで感染症専門医が解説。